PROBEN KÖNNEN SCHWIERIG SEIN, ABER MESSUNGEN KÖNNEN EINFACH SEIN.
Der pH-Wert ist ein entscheidender Parameter für viele Anwendungen.
Er ist ein grundlegender Parameter in der Lebensmittelindustrie, für die Optimierung der Vernickelung oder Verkupferung, für die Gewährleistung optimaler Bedingungen für ein gesundes Pflanzenwachstum und vieles mehr.
Der Grund dafür ist, dass der pH-Wert viele biologische und chemische Prozesse beeinflusst, wie die Vermehrung und das Überleben von Mikroorganismen, die Aktivität von Enzymen, chemische Reaktionen und Gleichgewichte, die Löslichkeit von Salzen usw.
Am häufigsten (und auch am genauesten) wird der pH-Wert mit einem pH-Meter mit einer Glaselektrode gemessen. Richtige und stabile Werte zu erhalten, kann jedoch schwierig sein, insbesondere bei einigen Proben (wie Lebensmittel, Erde, Cremes, Farben, Proben mit hohem pH-Wert usw.).
Es ist wichtig zu verstehen, was der pH-Wert bedeutet, wie eine pH-Elektrode funktioniert und wie die Messung durch Verwendung der richtigen Elektrode erleichtert werden kann.
Hanna Instruments ist ein führender Hersteller von pH-Elektroden und bietet eine große Auswahl an Elektroden für spezifische Anwendungen.
Petrochemische Industrie
Hanna Photometrische Elektroden zur Verwendung mit unseren
automatische potentiometrische Titratoren
1. Was ist der pH-Wert?
Der pH-Wert ist ein Maß dafür, wie viele aktive Wasserstoffionen in einer Probe vorhanden sind. In der Praxis wird die Konzertierung häufiger anstelle der Aktivität verwendet.
Einfacher ausgedrückt ist der pH-Wert ein Maß dafür, wie sauer oder wie alkalisch eine wässrige Lösung ist.
Der Begriff „pH“ steht für „pondus hydrogenii“ oder „das Wasserstoffpotenzial“ und wurde erstmals 1909 von dem dänischen Biochemiker Soren Peter Lauritz Sorensen eingeführt.
Während seiner Forschungen musste er oft messen, wie sauer die Probe ist, und fand es bequemer, die Wasserstoffionenkonzentration in der dekadischen logarithmischen Skala anzugeben (z. B. 0,0000001 mol/L H+ ergibt pH 7). Der pH-Wert wurde dann wie folgt definiert [1]:


a = Aktivität
c = Konzentration
H+ = Wasserstoff-Ion
Der pH-Wert wird also auf einer logarithmischen Skala von 0 bis 14 gemessen, wobei 7 neutral ist (Abbildung 1).
Wird dem Wasser eine so genannte Säure zugesetzt, erhöht sich die Wasserstoffionenkonzentration und der pH-Wert sinkt unter 7. Umgekehrt verringert eine als Base bezeichnete Substanz die Wasserstoffionenkonzentration und der pH-Wert steigt über 7. Das bedeutet, dass jede Lösung unter pH 7 sauer ist und jede Lösung über 7 alkalisch ist. Da wir den dekadischen Logarithmus verwenden, bedeutet 1 pH weniger eine Verzehnfachung der Aktivität von H+. [2]


2. Wie funktioniert eine pH-Elektrode?
Eine Glaselektrode oder eine pH-Elektrode ist eine Art ionenselektive Elektrode – sie ist selektiv für die Messung von Wasserstoff-Ionen. Für die potentiometrische pH-Messung werden die folgenden Teile benötigt:
- Referenzelektrode, am gebräuchlichsten ist die Silberchlorid-Halbzelle (mit AgCl beschichteter Silberdraht in Kontakt mit gesättigter KCl-Lösung) – hat konstantes Potenzial
- Indikatorelektrode mit dem pH-sensitiven Glas – ändert das Potential in Abhängigkeit von der Konzentration des Analyten,
- mV-Meter – misst die Potenzialdifferenz zwischen der Referenz- und der Indikatorelektrode.
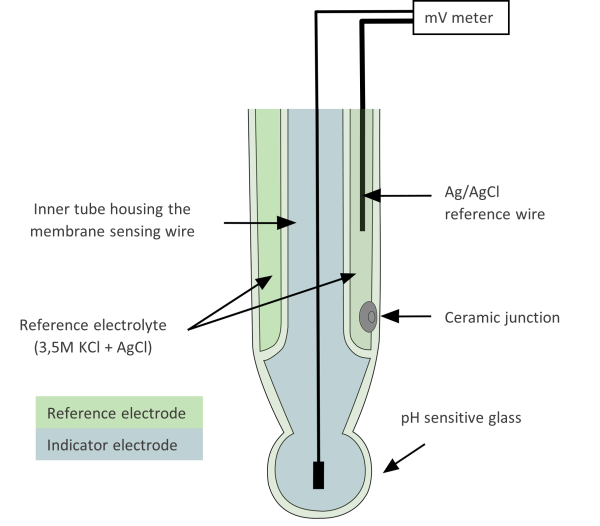

In der Regel wird eine kombinierte pH-Elektrode verwendet (Abbildung 2), die sowohl die Referenz- als auch die Indikatorelektrode enthält.
Der Teil der Elektrode, der für den pH-Wert empfindlich ist, ist der dünne Glaskolben oder Kegel am Boden der Indikatorelektrode. Auf der Oberfläche dieses empfindlichen Glases befinden sich negativ geladene Sauerstoffatome (aus SiO4), die positiv geladene Ionen geeigneter Größe – Wasserstoffionen (und auch Alkali-Ionen, jedoch mit geringerer Stärke) – binden können.
Wie viele Wasserstoffionen an die Oberfläche des empfindlichen Glases gebunden werden, hängt von der Aktivität (Konzentration) der Wasserstoffionen in der Probe ab. Wenn sich Wasserstoffionen an das pH-empfindliche Glas binden, wird ein elektrisches Potenzial erzeugt. Durch Ablesen dieses Potenzials mit einem mV-Meter kann daher der pH-Wert anhand der Nernst-Gleichung [2] berechnet werden:
E = Potential in mV
E0 = von der Referenzelektrode erzeugtes elektrisches Potenzial
β = die Auswirkung von Austrocknung, Verschmutzung, Kratzern usw. auf die Glasmembran
Ein weiterer wichtiger Bestandteil einer Elektrode ist die Kontaktstelle, die den Kontakt zwischen der Lösung in der Bezugselektrode (dem Elektrolyten, gesättigtes KCl) und der Probe ermöglicht. Der Elektrolyt entweicht aus der Referenzelektrode in die Probe, wodurch der Stromkreis geschlossen und Messungen möglich werden. Je stärker der Elektrolyt fließt, desto besser ist die Reaktion der Elektrode. [2]
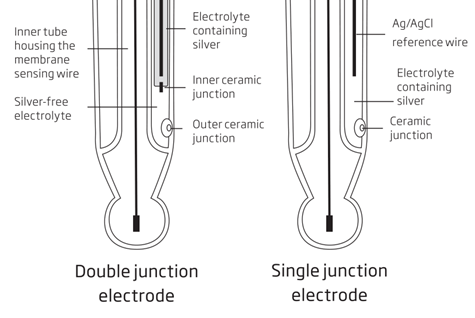
Bei Standard-Einkomponentenelektroden befindet sich die Bezugselektrode in direktem Kontakt mit der Probe (Abbildung 3). Das in der Referenzelektrode enthaltene Silberchlorid kann in der Probe schwer löslich sein, so dass sich bei Kontakt mit der Probe ein Niederschlag auf der Außenseite der Verbindungsstelle bildet, was zu abweichenden Messwerten führt. Unter ungünstigen Bedingungen (hoher Druck, hohe Temperatur, hohe Leitfähigkeit) kann sich der Elektrolytfluss auch umkehren, was zur Verunreinigung der Referenzhalbzelle und zum vollständigen Ausfall der Elektrode führt.
Doppelseitige Elektroden haben, wie der Name schon sagt, zwei Anschlüsse (Abbildung 3). Diese Elektroden haben ein zusätzliches Fach für die Referenzelektrode mit der inneren Verbindung. Der Zwischenbereich ist silberfrei und unempfindlich gegen Verunreinigungen, was die Langlebigkeit der Elektrode erhöht.

Warum müssen pH-Elektroden kalibriert werden?
Die Werte E0 und β in der Nernst-Gleichung hängen vom Zustand der Glasmembran (Hydratationsgrad, Ablagerungen, Kratzer usw.) und der Verbindungsstelle (Verstopfungsgrad) ab.
Die Berechnung dieser Werte wäre in der Praxis unmöglich, und die Veränderungen sind für die Ergebnisse zu signifikant. Nach Kalibrierung der pH-Elektrode mit Lösungen eines bekannten Wertes (vorzugsweise mit mindestens zwei) werden die Messungen entsprechend angepasst.
Warum müssen pH-Elektroden gewartet werden?
Es ist wichtig zu verstehen, dass Wasserstoffionen nur an die Glasmembran binden können, wenn diese hydratisiert ist. Aus diesem Grund sollte die Elektrode in der HI70300 Aufbewahrungslösung gelagert werden, die die Oberfläche der Elektrode hydratisiert und für Messungen bereit hält (Abbildung 4).


Wasserstoffionen können sich auch nicht an die Oberfläche binden, wenn dort (organische oder anorganische) Ablagerungen vorhanden sind. Die Qualität der Messungen hängt davon ab, wie groß die für die Codierung zur Verfügung stehende Fläche ist.
Die Reinigung mit dem HI7061 Allzweckreiniger oder einer anwendungsspezifischen Reinigungslösung entfernt die Ablagerungen und stellt die Elektrode wieder her (Abbildung 5).


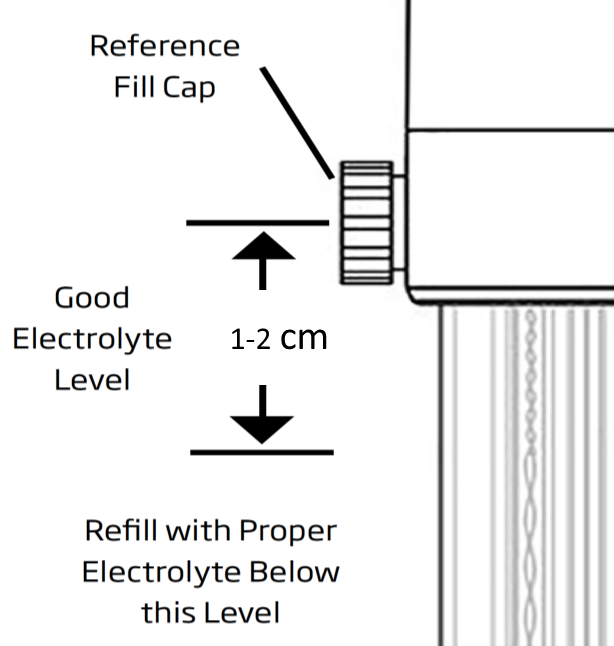

Der Elektrolytspiegel in der Bezugselektrode sollte 1-2 cm unterhalb der Einfüllöffnung gehalten werden, um einen angemessenen Druck für den Elektrolytabfluss aufrechtzuerhalten (Abbildung 6).
Vor den Messungen sollten die Elektrolytstände überprüft und bei Bedarf mit dem Elektrolyt HI7082 für Doppelkontaktelektroden oder HI7072 für Einfachkontaktelektroden aufgefüllt werden. Und bei den Messungen ist es wichtig, dass die Kappe locker oder offen ist.
Wie kann man den Zustand der pH-Elektrode überprüfen?
Um zu prüfen, ob die Elektrode in einem guten Zustand ist, sollten der Offset und die Steilheit bestimmt werden.
Der Offset ist der mV-Wert, der in einer Lösung mit pH 7,0 gemessen wird. Theoretisch sollte dieser Wert 0 mV betragen, aber in der Praxis ist ein Offset von ± 30 mV akzeptabel.
Die Steilheit kann bestimmt werden, indem der mV-Wert in Lösungen mit pH 7,0 und pH 4,0 (oder pH 10,0) gemessen und die absolute mV-Differenz berechnet wird.
Aus der Nernst-Gleichung geht hervor, dass dieser Unterschied 59,16 mV * 3 (der Unterschied im pH-Wert) = 177,48 mV betragen sollte, aber 150 mV bis 186 mV ist eine akzeptable Steigung.
3. Messung des pH-Werts von schwierigen Proben
Bei der Messung des pH-Werts mit einer Glaselektrode können einige Schwierigkeiten auftreten. Zunächst müssen wir sicherstellen, dass die Elektrode ordnungsgemäß gewartet (gereinigt, hydriert, nachgefüllt) und mit frischen Puffern kalibriert wurde. Bleiben die Probleme bestehen, ist die Elektrode für die Messung des pH-Wertes in unserer Probe nicht geeignet. Einige der häufigsten Probleme sind:
- wenn aufgrund chemischer/physikalischer Eigenschaften der Probe oder der Verstopfung von Verbindungsstellen nicht genügend Elektrolyt fließt,
- wenn die Probe halbfest oder fest ist,
- wenn eine erhebliche Konzentration von Natrium- oder anderen Alkali-Ionen vorhanden ist,
- wenn es sich um eine Probe mit HF handelt,
- wenn wir Probenehmer mit hohen/niedrigen Temperaturen messen oder
- wenn Lärm aus der Umgebung auftritt.
Hanna Instruments bietet Lösungen für all diese Probleme mit speziellen Anschlüssen, Spitzen, Glasarten und Gehäusedesigns.
3.1. Niedriger Elektrolytfluss
Beispiele:
- Proben mit niedriger Leitfähigkeit (z. B. Trinkwasser, Proben mit weniger als 100 μS/cm)
- Proben mit hoher Leitfähigkeit (z. B. Solen, Meerwasser, starke Säuren, starke Basen)
- viskose Proben (z. B. Farben, Kosmetika, Pasten, Emulsionen)
Ein ausreichender Elektrolytfluss von der Referenzelektrode in die Probe durch die Verbindungsstelle ist entscheidend für stabile Messwerte.
In Fällen, in denen sich der Bezugselektrolyt und die Probe in ihrer Zusammensetzung stark unterscheiden, ist dieser Fluss begrenzt, und ein Phänomen, das als Übergangspotenzial bezeichnet wird, hat erhebliche Auswirkungen auf die Messungen.
Standardelektroden haben einen keramischen Übergang, der keinen ausreichenden Elektrolytfluss gewährleistet, wenn der pH-Wert von Proben mit niedriger Leitfähigkeit, hoher Leitfähigkeit oder zähflüssigen Proben gemessen wird. Durch die Verwendung von Elektroden mit mehreren keramischen Verbindungsstellen wird die Durchflussrate erhöht und die Messwerte stabilisiert.
Die Hanna Instruments HI10530 pH-Doppelsperrschicht-Elektrode mit einer dreifachen keramischen Sperrschicht an der äußeren Sperrschicht (Abbildung 7) wurde für zuverlässige pH-Messungen in Proben mit niedriger Leitfähigkeit und Viskosität entwickelt und zeichnet sich durch eine Elektrolytflussrate von 40 bis 50 µL/Stunde aus (im Vergleich zu 15 bis 20 µL/Stunde bei einer Standardelektrode).
Darüber hinaus verbessert der Niedertemperatur-Glastyp mit niedrigerer Impedanz die Qualität der pH-Messungen in solchen Proben.
Die Hanna Instruments HI10430 pH-Doppelsperrschicht-Elektrode mit doppelter keramischer Sperrschicht (Abbildung 8) ist ideal für Anwendungen mit Proben mit hoher Leitfähigkeit oder konzentrierten Proben, die einen Elektrolytdurchfluss von 30 bis 40 µL/Stunde aufweisen.
Das Doppelkontaktsystem schützt auch die Referenzelektrode vor Verunreinigungen.
3.2. Verstopfte Abzweigung
Beispiele:
- „schmutzige“ Proben mit hohem Feststoffanteil (z. B. Wein, Saft, Maische, Würze)
- Fett
- Proteingehalt (z. B. Milch, Fleisch, Käse und andere Lebensmittelproben)
Wie bereits erwähnt, schließt der Elektrolyt, der von der Referenzelektrode in die Proben austritt, den Stromkreis und ermöglicht die Messung. Jede Verstopfung der Verbindungsstelle führt zu unregelmäßigen und instabilen Messwerten.
„Verschmutzte“ Proben, die einen hohen Gehalt an Feststoffen, Fetten, Proteinen usw. aufweisen, können die herkömmlichen keramischen Verbindungsstellen schnell verstopfen und die Elektrode unbrauchbar machen.
Die Wahl einer Elektrode mit einem speziellen Anschlussdesign, das gegen Verstopfung resistent ist (z. B. Clogging Prevention System, Tuchanschluss oder offener Anschluss), verlängert die Lebensdauer der Elektrode.
Die pH-Elektrode HI1048 von Hanna Instruments verfügt über die Clogging Prevention System (CPS)-Technologie (Abbildung 9) und ist für die pH-Analyse von Wein, Most und Saft konzipiert.
Die CPS-Technologie nutzt die Porosität von gemahlenem Glas in Verbindung mit einer PTFE-Hülse, um ein Verstopfen der Verbindungsstelle zu verhindern.
Das geschliffene Glas lässt die Flüssigkeit gut fließen, während die PTFE-Hülle Feststoffe abweist.
Eine weitere Messstelle, die sich für die Messung des pH-Werts von Proben mit einem hohen Anteil an Böden eignet, ist die Messstelle mit einziehbarem Tuch.
In diesem Fall kann die Kreuzung durch einfaches Herausziehen von ca. 3 mm von der Verbindungsstelle entfernt.
Die Hanna Instruments FC214 pH-Elektrode (Abbildung 10) verfügt über eine Tuchverbindung und ist ideal für die Analyse von Maische und Würze bei der Bierherstellung.
Die pH-Elektroden der Serie Foodcare von Hanna Instruments zeichnen sich durch eine offene Kontaktstelle aus.
Bei dieser Art von Verbindung befindet sich eine feste Gel-Grenzfläche (Viscolen) zwischen der Probe und der internen Ag/AgCl-Referenz.
Diese Schnittstelle macht sie undurchlässig für Verstopfungen, was zu einer schnellen Reaktion und stabilen Messwerten führt.
Außerdem verhindert diese Art von Verbindung eine Kontamination der Proben, was bei der Untersuchung von Lebensmitteln von entscheidender Bedeutung ist.
3.3. Feste und halbfeste Proben
Beispiele:
- halbfeste Proben (z. B. Joghurt, Käse, Fleisch, Cremes, Bodenproben)
- feste Proben (z. B. Haut, Leder, Agarplatten, Papier)
Die herkömmlichen kugelförmigen pH-Elektroden wurden für wässrige Proben entwickelt, da sie eine große Oberfläche für die Probeninteraktion bieten.
Mit dieser Art von Spitzenform ist es jedoch schwierig, in halbfeste Proben einzudringen oder mit festen Proben in Kontakt zu kommen. Elektroden mit konisch oder flach geformten Spitzen ermöglichen eine direkte Messung.
Die Prüfung von halbfesten Proben wird durch konisch geformte Spitzenelektroden erleichtert. Diese Art von Spitze ermöglicht das Eindringen und die direkte Messung des pH-Wertes in Proben wie Joghurt, Käse, Fleisch, Sahne, Erde usw.
Hanna Instruments bietet eine große Auswahl an konischen Elektroden an, die für spezifische Proben entwickelt wurden (Abbildung 11).










Abbildung 11: Hanna Instruments Elektroden
Bei festen Proben, bei denen ein Eindringen in die Probe nicht möglich ist, sollte der Oberflächenkontakt mit einer flach geformten Elektrode optimiert werden.
Die Elektrode HI1414 von Hanna Instruments mit einer flach geformten Spitze (Abbildung 12) ist für Oberflächenmessungen des pH-Werts auf Haut, Leder, Agarplatten, Papier usw. bestimmt.
3.4. Proben mit hohem pH-Wert
Beispiele:
- Proben mit einem pH-Wert von über 12 (z. B. Waschmittel, Seifenwasser, Haushaltsreiniger, starke Basen)
Das pH-empfindliche Glas ist nicht streng selektiv für Wasserstoffionen.
Alkali-Ionen, insbesondere Natrium-Ionen, können sich ebenfalls an die Glasoberfläche binden, allerdings mit geringerer Stärke und in den meisten Fällen ohne nennenswerte Auswirkungen auf die pH-Messungen.
In Proben mit hohem pH-Wert ist die Wasserstoffionenkonzentration im Vergleich zur Alkaliionenkonzentration sehr gering, und die Menge der an die Glasoberfläche gebundenen Alkaliionen führt zu erheblichen Veränderungen des Lesepotenzials.
Der angezeigte pH-Wert ist daher niedriger als er tatsächlich ist. Die Differenz zwischen den theoretischen und den gemessenen Werten wird als Alkalifehler bezeichnet.
Das Hochtemperaturglas von Hanna Instruments minimiert Alkalifehler in stark alkalischen Lösungen.
Bei einem pH-Wert von 13 in einer Lösung mit einer Natriumkonzentration von 1,0 M beträgt der Alkalifehler für ein Hochtemperaturglas 0,15 pH, im Vergleich zu 0,43 pH für Allzweckglas und über 0,79 pH für Niedertemperaturglas.
3.5. Proben mit Fluorwasserstoffsäure
Beispiele:
- fluoridhaltige Laborreagenzien und analytische Standards
Fluorwasserstoffsäure kann Glas schnell auflösen. Die Elektrode HI1143 von Hanna Instruments verwendet HF-beständiges Glas für aggressive Anwendungen, die Fluoridionen (bis zu 2 g/L) enthalten.
Mit diesem Glas hergestellte Elektroden halten zehnmal länger als Elektroden, die mit Standard-pH-Glasrezepturen hergestellt wurden (von 10 bis 100 Tagen). Darüber hinaus schützt die Doppelanschlusskonstruktion die Kontamination der Referenzelektrode.
3.6. Proben mit hoher/niedriger Temperatur
Beispiele:
- gekühlte Lebensmittel
- Pasteurisierung
- Würzekochen
Bei niedrigen Temperaturen liefern Elektroden mit einem Glas mit hoher Impedanz bei niedrigen Temperaturen sehr verrauschte und unregelmäßige Signale. Hanna Instruments Elektroden mit NIEDRIGEM Temperaturglas haben eine niedrige Impedanz und ermöglichen stabile Messungen bei niedrigeren Temperaturen.
Bei erhöhten Temperaturen kann sich das Glas jedoch leicht auflösen, was die Lebensdauer und Leistung der Elektrode verkürzt. Die Elektroden von Hanna Instruments mit Hochtemperaturglas sind für einen längeren Einsatz bei hohen Temperaturen ausgelegt. Mit dem widerstandsfähigeren Glas sind Messungen bei erhöhten Temperaturen genau und mit hervorragenden Ansprechzeiten möglich.
3.7. Proben mit elektrischen Strömen
Beispiele:
- galvanische Bäder
- Kühltürme
- Heizkessel
- Schwimmbäder
Elektrische Ströme in der Probe können die Spannung der Referenz-Halbzelle beeinflussen, die über den Flüssigkeitsübergang mit der Probe verbunden ist. In diesem Fall nimmt die Referenzelektrode die elektromagnetischen Felder auf und die Messung des pH-Wertes wird verändert.
Ein Anpassungsstift ist eine differentielle Messtechnik, die dazu dient, Masseschleifen und Gleichtaktstörungen für ein Messsystem zu eliminieren und so Strom-/Magnetfelder von der Referenzelektrode zu isolieren. Hanna stellt eine Reihe von Modellen mit dem passenden Stiftdesign für sichere und präzise pH-Messungen her.
Dieses Problem lässt sich auch durch die Verwendung von Elektroden mit Titankörper lösen (Abbildung 13). Der Titankäfig wirkt wie ein Faradayscher Käfig und schirmt das Innere der Elektrode vom Außenlärm ab.
Sie sind sich nicht sicher, welche Elektrode die beste für Ihre Probe ist?
Wenden Sie sich an einen technischen Spezialisten von Hanna unter info@hannaservice.eu oder verwenden Sie unser Kontaktformular.
REFERENZEN:
- Jensen, William B. (2004). „The Symbol for pH“ (PDF). Journal of Chemical Education.
- Harris C. Daniel (2010). Quantitative Chemical Analysis, 8th Edition. H. Freeman and Company, New York


With Great Product
Come Great Results









